CDE更新共性问题:这种情况,可以继续按照改良型新药申报
CDE
2025/07/07 13:44:49
7月1日,国家药监局药品审评中心官网更新一条受理共性问题,对改良型新药申报相关问题进行解答。
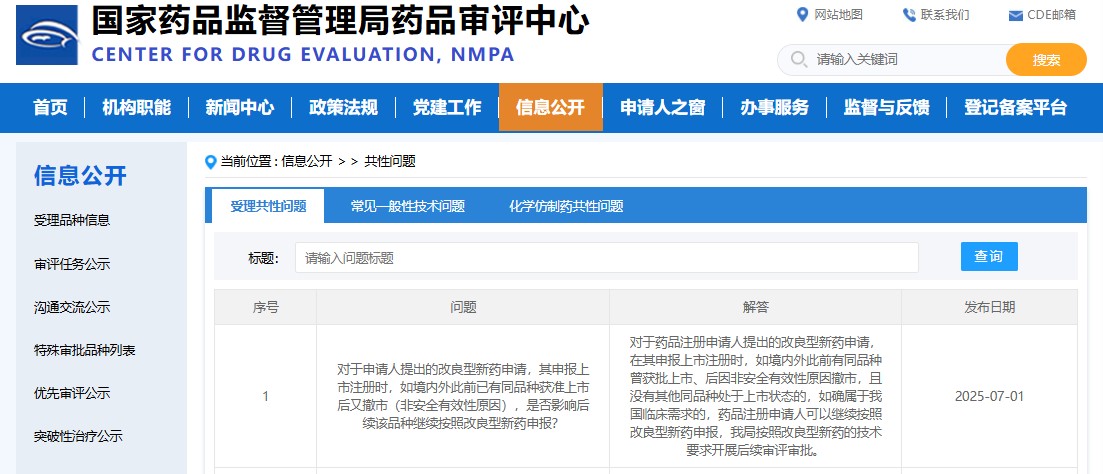
问:对于申请人提出的改良型新药申请,其申报上市注册时,如境内外此前已有同品种获准上市后又撤市(非安全有效性原因),是否影响后续该品种继续按照改良型新药申报?
答:对于药品注册申请人提出的改良型新药申请,在其申报上市注册时,如境内外此前有同品种曾获批上市、后因非安全有效性原因撤市,且没有其他同品种处于上市状态的,如确属于我国临床需求的,药品注册申请人可以继续按照改良型新药申报,我局按照改良型新药的技术要求开展后续审评审批。